Chapitre 4. Acides, bases et réactions chimiques
I. Quelle réaction se produit entre une solution acide et une solution basique ?
Activité 1. Comment traiter les déchets acides ou basiques ?
Regarder la vidéo ci-dessous pour préparer l'activité 1 :

A RETENIR :
Lorsqu’on ajoute une solution basique dans une solution acide, le pH de la solution acide augmente.
Les industriels utilisent cette technique appelée neutralisation de manière à obtenir des solutions neutres (pH = 7) avant de les rejeter à l’égout.
Les ions hydrogène réagissent avec les ions hydroxyde pour donner de l’eau :

II. Quelle réaction se produit entre le fer et l'acide chlorhydrique ?
Activité 2. Evaluation expérimentale
A RETENIR :
Le fer (Fe) réagit avec l’acide chlorhydrique (H+ ; Cl-) pour donner du dihydrogène (H2) et une solution de chlorure de fer II (Fe2+ ; Cl-). Le dihydrogène peut également être produit lors de la réaction entre un autre métal que le fer et l'acide chlorhydrique.
Il y a eu une transformation chimique. Des réactifs ont disparu (ions hydrogène et fer) et des produits sont apparus (dihydrogène et ions fer II). Les ions chlorure sont des ions spectateurs qui ne participent pas à la transformation.
Bilan de la transformation chimique :


Pour s'entraîner
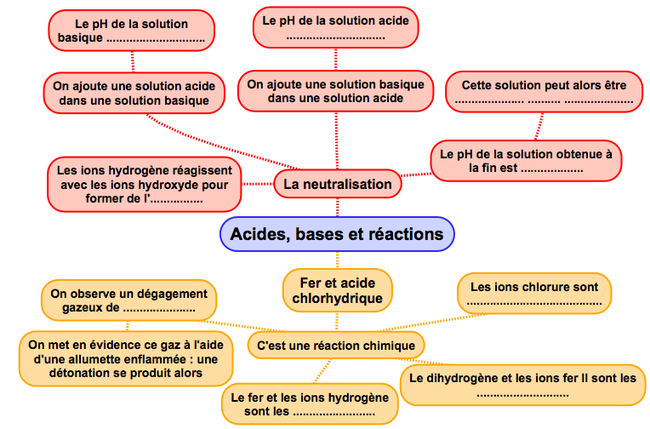
Organiser ses connaissances en complétant la carte mentale :
Tester ses connaissances en faisant le quizz.
S'évaluer avec l'évaluation blanche :
Ce site a été conçu avec Jimdo. Inscrivez-vous gratuitement sur https://fr.jimdo.com
